Osnovne informacije
- Lokacija
- Splitsko-dalmatinska, Split, Sućidar
- Stanje
- novo
Opis oglasa
Kositrov(II) klorid dihidrat, također poznat kao kositrov klorid , bijela je kristalna krutina s formulom SnCl2 . Tvori stabilan dihidrat, ali vodene otopine podliježu hidrolizi, osobito ako su vruće. SnCl2 se široko koristi kao redukcijsko sredstvo (u kiseloj otopini), te u elektrolitičkim kupkama za kalajisanje. Kositrov(II) klorid ne smije se miješati s drugim kositrovim kloridom; kositar(IV) klorid ili kositrov klorid (SnCl4 ).
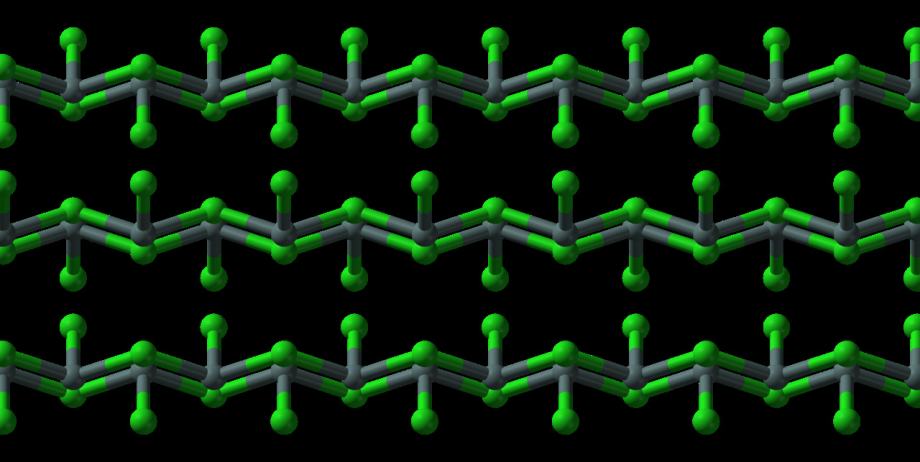
SnCl2 ima usamljeni par elektrona, tako da je molekula u plinskoj fazi savijena. U čvrstom stanju, kristalni SnCl2 tvori lance povezane preko kloridnih mostova kao što je prikazano. Dihidrat je također trokoordinatan, pri čemu je jedna voda usklađena s limenom, a druga voda koordinirana s prvom. Glavni dio molekule slaže se u dvostruke slojeve u kristalnoj rešetki, s "drugom" vodom u sendviču između slojeva.
Kositrov (II) klorid može se otopiti u manje od svoje vlastite mase vode bez prividne razgradnje, ali kako se otopina razrijedi, dolazi do hidrolize da nastane netopiva bazična sol:
Stoga, ako se trebaju upotrijebiti bistre otopine kositrovog (II) klorida, mora se otopiti u klorovodičnoj kiselini (obično istog ili većeg molariteta kao kositrov klorid) kako bi se održala ravnoteža prema lijevoj strani (pomoću Le Chatelierove princip ). Otopine SnCl 2 također su nestabilne prema oksidaciji zrakom:
Postoji mnogo takvih slučajeva u kojima kositar(II) klorid djeluje kao redukcijsko sredstvo, reducirajući soli srebra i zlata u metal, a soli željeza(III) u željezo(II), na primjer:
Otopine kositar(II) klorida također mogu poslužiti jednostavno kao izvor iona Sn 2+ , koji mogu tvoriti druge spojeve kositar(II) reakcijom taloženja . Na primjer, reakcija s natrijevim sulfidom proizvodi smeđi/crni kositar(II) sulfid :
50g - 20€
100g - 40€
SnCl2 ima usamljeni par elektrona, tako da je molekula u plinskoj fazi savijena. U čvrstom stanju, kristalni SnCl2 tvori lance povezane preko kloridnih mostova kao što je prikazano. Dihidrat je također trokoordinatan, pri čemu je jedna voda usklađena s limenom, a druga voda koordinirana s prvom. Glavni dio molekule slaže se u dvostruke slojeve u kristalnoj rešetki, s "drugom" vodom u sendviču između slojeva.
Kositrov (II) klorid može se otopiti u manje od svoje vlastite mase vode bez prividne razgradnje, ali kako se otopina razrijedi, dolazi do hidrolize da nastane netopiva bazična sol:
Stoga, ako se trebaju upotrijebiti bistre otopine kositrovog (II) klorida, mora se otopiti u klorovodičnoj kiselini (obično istog ili većeg molariteta kao kositrov klorid) kako bi se održala ravnoteža prema lijevoj strani (pomoću Le Chatelierove princip ). Otopine SnCl 2 također su nestabilne prema oksidaciji zrakom:
Postoji mnogo takvih slučajeva u kojima kositar(II) klorid djeluje kao redukcijsko sredstvo, reducirajući soli srebra i zlata u metal, a soli željeza(III) u željezo(II), na primjer:
Otopine kositar(II) klorida također mogu poslužiti jednostavno kao izvor iona Sn 2+ , koji mogu tvoriti druge spojeve kositar(II) reakcijom taloženja . Na primjer, reakcija s natrijevim sulfidom proizvodi smeđi/crni kositar(II) sulfid :
50g - 20€
100g - 40€
Karta
Napomena: Prikazana je približna lokacija
Mongostin1
Svi oglasi ovog oglašivača
Korisnik je verificirao broj telefona u državi: Hrvatska
Korisnik nije trgovac te na njega nisu primjenjive EU odredbe o zaštiti potrošača
- Adresa: 21000 Split, Splitsko-dalmatinska, Hrvatska
-
- Oglas objavljen
- 02.12.2025. u 17:16
- Do isteka još
- Oglas prikazan
- 990 puta
Mongostin1
Svi oglasi ovog oglašivača
Korisnik je verificirao broj telefona u državi: Hrvatska
Korisnik nije trgovac te na njega nisu primjenjive EU odredbe o zaštiti potrošača
- Adresa: 21000 Split, Splitsko-dalmatinska, Hrvatska
-